Металлы – это класс химических элементов, которые играют колоссальную роль в нашей жизни. От строительства небоскребов до производства электроники, металлы окружают нас повсюду. Разнообразие их свойств поражает воображение, и среди этого многообразия выделяются два элемента, занимающие противоположные позиции по плотности: самый тяжелый и самый легкий металлы. Понимание их характеристик и применений открывает захватывающие перспективы в науке и технике. Эта статья посвящена изучению этих удивительных элементов, их свойств, истории открытия и перспектив использования.
Осмий: Самый тяжелый металл
Осмий (Os) – это переходный металл платиновой группы, известный своей невероятной плотностью. Он был открыт в 1803 году английским химиком Смитсоном Теннантом вместе с иридием при изучении остатка, полученного после растворения платины в царской водке (смеси концентрированных азотной и соляной кислот). Название «осмий» происходит от греческого слова «osme», что означает «запах», из-за характерного резкого запаха тетраоксида осмия (OsO4).
Осмий – это твердый, хрупкий, серебристо-белый металл с синеватым оттенком. Он является одним из самых редких элементов в земной коре, его содержание составляет около 0,001 ppm. Осмий обладает исключительной химической стойкостью, устойчив к воздействию большинства кислот и щелочей. Однако при нагревании на воздухе он окисляется, образуя летучий и токсичный тетраоксид осмия.
Физические и химические свойства осмия
Главной особенностью осмия является его чрезвычайно высокая плотность – 22,59 г/см3. Это делает его самым плотным известным элементом. Температура плавления осмия составляет 3033 °C, а температура кипения – 5012 °C. Он обладает высокой твердостью и модулем упругости, что делает его очень устойчивым к деформации.
Химически осмий относительно инертен, но при высоких температурах он реагирует с кислородом, галогенами и некоторыми другими элементами. Он образует соединения в различных степенях окисления, от -2 до +8, наиболее распространенной из которых является +4. Тетраоксид осмия (OsO4) является сильным окислителем и используется в органическом синтезе и гистологии.
Применение осмия
Благодаря своей высокой твердости и износостойкости, осмий используется в сплавах для изготовления:
- Электрических контактов.
- Деталей приборов, работающих в условиях высоких нагрузок.
- Иголок для граммофонов (в прошлом).
Осмий также используется в качестве катализатора в некоторых химических реакциях. Тетраоксид осмия находит применение в микроскопии для окрашивания биологических образцов и в органическом синтезе для дигидроксилирования олефинов.
Токсичность и меры предосторожности
Тетраоксид осмия является очень токсичным и опасным веществом. Он вызывает раздражение кожи, глаз и дыхательных путей. Вдыхание паров тетраоксида осмия может привести к серьезным повреждениям легких и глаз. При работе с осмием и его соединениями необходимо соблюдать строгие меры предосторожности, использовать защитное оборудование и обеспечивать хорошую вентиляцию.
Литий: Самый легкий металл
Открытие и общие характеристики
Литий (Li) – это щелочной металл, известный своей чрезвычайно низкой плотностью. Он был открыт в 1817 году шведским химиком Юханом Арфведсоном при анализе минерала петалита. Название «литий» происходит от греческого слова «lithos», что означает «камень», поскольку литий был впервые обнаружен в минеральном, а не растительном или животном источнике.
Литий – это мягкий, серебристо-белый металл, который легко режется ножом. Он является самым легким из всех металлов и самым легким твердым элементом. Литий очень реакционноспособен и легко взаимодействует с водой, кислородом и азотом. Поэтому его хранят под слоем минерального масла или в инертной атмосфере.
Физические и химические свойства лития
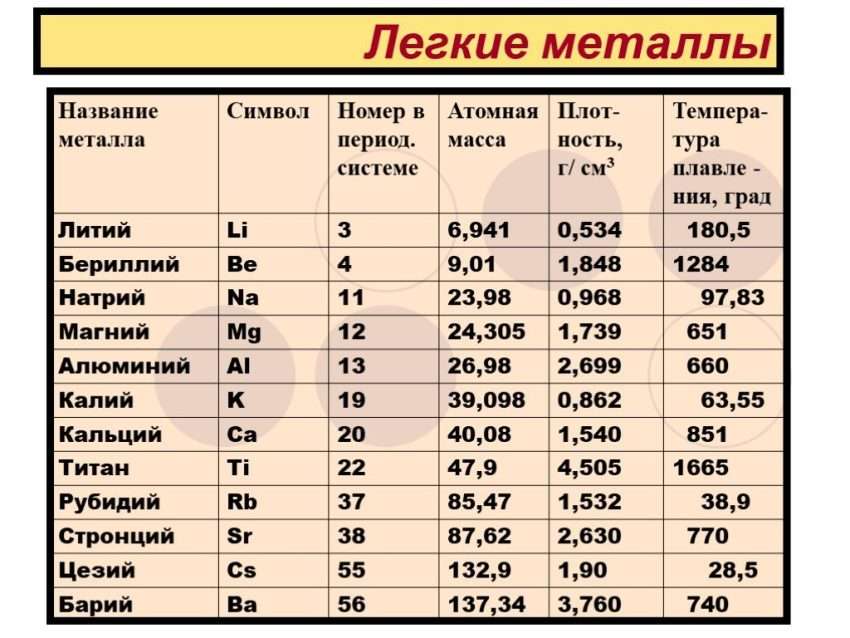
Плотность лития составляет всего 0,534 г/см3, что примерно вдвое меньше плотности воды. Температура плавления лития составляет 180,54 °C, а температура кипения – 1342 °C. Он обладает высокой теплопроводностью и электропроводностью.
Литий является очень активным металлом и легко отдает свой единственный валентный электрон, образуя положительно заряженный ион Li+. Он бурно реагирует с водой, образуя гидроксид лития и водород. Литий также реагирует с азотом при комнатной температуре, образуя нитрид лития. Он образует множество соединений с различными элементами, включая галогены, кислород и серу.
Применение лития
Благодаря своим уникальным свойствам, литий находит широкое применение в различных областях:
- Аккумуляторы: Литий-ионные аккумуляторы используются в мобильных телефонах, ноутбуках, электромобилях и других портативных устройствах.
- Смазки: Литиевые смазки используются в автомобильной промышленности и других областях, где требуется высокая термостойкость и водостойкость.
- Медицина: Карбонат лития используется для лечения биполярного расстройства.
- Металлургия: Литий используется в качестве добавки к алюминиевым сплавам для повышения их прочности и коррозионной стойкости.
- Ядерная энергетика: Изотоп литий-6 используется для производства трития, который является компонентом термоядерного топлива.
Меры предосторожности
Литий – это легковоспламеняющийся металл, и его пыль может образовывать взрывоопасные смеси с воздухом. При работе с литием необходимо соблюдать меры предосторожности, использовать защитное оборудование и избегать контакта с водой и окислителями. Соединения лития могут быть токсичными при проглатывании или вдыхании.
Сравнение осмия и лития
Осмий и литий представляют собой два полюса в мире металлов. Осмий – это самый тяжелый и плотный металл, обладающий исключительной твердостью и химической стойкостью. Литий – это самый легкий металл, обладающий высокой реакционной способностью и уникальными электрохимическими свойствами. Эти два элемента имеют совершенно разные применения, но оба играют важную роль в современной науке и технике.
| Характеристика | Осмий | Литий |
|---|---|---|
| Плотность (г/см3) | 22,59 | 0,534 |
| Температура плавления (°C) | 3033 | 180,54 |
| Температура кипения (°C) | 5012 | 1342 |
| Реакционная способность | Низкая (кроме взаимодействия с кислородом при нагревании) | Высокая |
| Применение | Электрические контакты, детали приборов, катализаторы | Аккумуляторы, смазки, медицина, металлургия, ядерная энергетика |
Будущее применения самых тяжелого и легкого металла
Исследования в области материаловедения постоянно открывают новые возможности для применения осмия и лития. Осмий может найти применение в новых сплавах с улучшенными характеристиками, а также в нанотехнологиях. Литий играет ключевую роль в развитии электромобилей и накопителей энергии, и его потребность будет только расти в будущем.
Поиск новых месторождений и разработка более эффективных методов добычи этих элементов являются важными задачами для обеспечения устойчивого развития современной промышленности. Утилизация и переработка отходов, содержащих осмий и литий, также играют важную роль в сохранении природных ресурсов и снижении воздействия на окружающую среду.
Описание: Узнайте о свойствах и применении осмия и лития, **самых тяжелого и легкого металлов**, их роли в современной промышленности и перспективах на будущее.